Le spin de l’électron est un espion au sein de la matière carbonée car la RPE (Résonance Paramagnétique Électronique) est un outil très important pour analyser des sédiments vieux de plus 3,3 millions d’années. Le signal de résonance électronique sur un échantillon de très faible épaisseur montre qu’il existe de la matière organique extraterrestre dans ces sédiments. Un scénario est proposé : une pluie de micrométéorites dans une mer calme…
Source : L’Actualité chimique n° 452 (juin 2020) pp. 51-52
Le β-cyclocitral est un aldéhyde produit par oxydation du β-carotène par l’oxygène singulet ; Il s’oxyde dans les plantes en acide β-cyclocitrique qui augmente la tolérance au stress hydrique. Il est soluble dans l’eau, peu volatil et est alors un excellent agent phytostimulant pour augmenter la tolérance des cultures à la sécheresse. Des tests sur des plantes sont cités et un brevet est déposé par les auteurs depuis 2018.
Source : L’Actualité chimique n° 455 (octobre 2020) pp. 63-64
L’expression « hydrogène à faible empreinte carbone » est plutôt recommandée par le Journal officiel [1]. L’hydrogène jouera sans doute un rôle important dans la transition énergétique. Il possède en effet l’énergie massique la plus élevée des combustibles (1200 MJ/kg) soit trois fois celle de l’essence ; de plus son utilisation dans les piles à combustible avec l’oxygène ne forme en effet que de l’eau sans aucune émission de produits polluants et fait l’objet de nombreux articles et dossiers dans la presse. Il est aussi à ce jour le meilleur moyen de stocker massivement de l’énergie sur une longue durée ce qui permet de répondre à l’intermittence des énergies solaire et éolienne [2].
Mais actuellement 95% de l’hydrogène est produit à partir de combustibles fossiles notamment par vaporeformage du gaz naturel selon l’équation bilan : CH4 + 2 H2O → CO2 + 4 H2 avec une production de 10 tonnes de CO2 par tonne d’hydrogène ! [3] [4] [5]. Cette technique pourrait être maintenue si on la couplait à des unités de stockage de CO2 et/ou par une opération de pyrolyse à haute température (voir plus loin [13]).
1/ L’électrolyse de l’eau
Rappelons qu’à l’anode se dégage de l’oxygène et à la cathode de l‘hydrogène. C’est la production « propre » recommandée par l’Europe. En France mentionnons le lancement de la Fédération H2 (FRH2_21) du CNRS le 9 mars 2021 suivi d’un colloque dès juin 2021 [6] [7]. Mais encore faut-il que l’électricité nécessaire à l’électrolyse soit décarbonée donc issue d’énergies renouvelables ou d’énergie nucléaire. Cet été en Vendée la startup nantaise Lhyfe a produit pour la première fois au monde de l’hydrogène avec une capacité de 300 kg H2/jour par électrolyse d’eau de mer avec une électricité provenant des éoliennes terrestres voisines à Bouin. Une station de distribution va fonctionner prochainement à La Roche-sur-Yon avec un prix à la pompe comparable à un plein d’essence ! [8]
i) L’électrolyse alcaline utilise de la potasse à 40% car la conductivité de la potasse est supérieure à celle de la soude et l’élimination des impuretés des ions chlorures et sulfates y est plus aisée. Les électrodes sont en nickel. Les compartiments anodique et cathodique sont séparés par une membrane constituée de copolymère à base de tétrafluoroéthylène présentant des greffons sulfonates (SO3-) en bout de chaines, pour éviter tout mélange explosif car au-delà de 4% en volume de H2 dans l’oxygène le mélange devient explosif ! La température de fonctionnement est de l’ordre de 80°C. C’est la technique la plus avancée industriellement avec un coût d’investissement des électrolyseurs le plus faible actuellement de l’ordre de 600 euros/kW. La consommation électrique y est de 4,5 kWh/Nm3. Le prix de revient du Nm3 dépend bien sûr du prix du kWh et de l’amortissement de l’investissement (l’unité Nm3 est définie en note *). Des plateformes industrielles développées par la société McPhy Energy ont des puissances de plus de 100 MW ! [9]
ii) L’électrolyse en milieu acide dite PEM pour « proton membrane exchange » a un coût plus élevé actuellement de 900 euros/kW. La consommation électrique est du même ordre de grandeur : 4,5 kWh/Nm3. L’électrolyte solide à forte conductivité ionique est constitué d’un copolymère à base de tétrafluoroéthylène présentant des greffons sulfoniques acides (SO3H) en bout de chaine. La cathode est en carbone recouvert de platine. L’anode est en titane recouvert d’oxyde d’iridium ; ces revêtements sont nécessaires pour catalyser les réactions d’oxydo-réduction. L’anode est ici poreuse et permet de capter l’oxygène formé et diminue le risque d’explosion avec l’hydrogène. La température est voisine de celle utilisée en milieu alcalin. Des applications dans les sous-marins ou dans le spatial sont déjà réalisées. La société Hydrogenics (en partenariat avec l’Air Liquide) au Canada, envisage de produire par ce procédé jusqu’à 3000 t/an d’hydrogène ! [10]
iii) L’électrolyse de l’eau en phase vapeur est possible vers 800°C. L’augmentation de la température permet d’apporter de l’énergie pour dissocier la molécule d’eau ! La tension à appliquer entre électrodes n’est que de 0,8 V. La consommation électrique est aussi réduite à 3 kWh/Nm3. Cependant le coût d’investissement est plus élevé soit 2100 euros/kW. L’électrolyte est constitué d’une céramique zircone (oxyde de ziconium) ZrO2, mélangé avec de l’oxyde d’yttrium qui est conductrice d’ions oxyde (O2-). Schématiquement : l’oxydation anodique s’écrit 2 O2- → O2 + 4 e- et la réduction cathodique 2 H2O + 4 e- → O2- + 2 H2.
L’anode est en céramique de type pérovskite LSCF (lanthane, strontium, cobalt ferrite) et la cathode où se dégage H2 est un matériau composite céramique / métal (zircone yttriée/ nickel).
Pour atteindre la température de fonctionnement, on utilise un échange thermique avec une source de chaleur existante aux environs de 150°C (stations d’incinération, géothermie, sites industriels, eau du circuit de refroidissement des centrales nucléaires...), puis l’architecture système de l’électrolyseur permet de surchauffer la vapeur jusqu’à 800°C en récupérant la chaleur émise par effet Joule dans chaque cellule bien que la réaction d’électrolyse soit endothermique. L’avantage de cette technologie est aussi la réversibilité de l’installation (électrolyseur / pile à combustible). Des développements permettent actuellement des productions de 16 Nm3/h [11].
La startup Sylfen créée en 2015 par le CEA a utilisé ce type d’électrolyse incluse dans un procédé de chauffage pour des immeubles autonomes en énergie !
2/ Autres techniques
i) La technique de décarbonation directe du méthane (DMD) par voie plasma électrique revient à craquer du méthane à très haute température (2000°C) dans un réacteur à flux continu pour donner une coproduction de noir de carbone très valorisable industriellement et d’hydrogène très pur. Le procédé ici ne nécessite qu’à peine 2 kWh d’électricité par Nm3 d’hydrogène et ne s’accompagne d’aucun dégagement de CO2 ! Cette technique s’accompagne d’une quantité importante de noir de carbone (biochar) qu’il est nécessaire de valoriser par exemple dans divers matériaux (bétons, ciments, pneumatiques, câbles électriques, encres, peintures…) ou en agriculture pour augmenter la productivité des sols. Une première unité industrielle fonctionne depuis 2020 aux USA dans le Nebraska [12].
ii) La pyrolyse de la biomasse végétale vers 800 °C conduit par craquage à la coproduction de charbon de bois (le biochar) et de gaz de synthèse (CO + H2). Les réactions de craquage sont endothermiques mais l’apport de chaleur rend le processus autothermique. Le bilan carbone est ici diminué car le charbon produit ici, ne provient que de la biomasse : chaque kg d’hydrogène s’accompagne de la production de 5 kg de biochar (soit une séquestration équivalente de 15 kg de CO2 !) qui peut être enfoui pour valorisation du sol. La société Haffner Energy a réalisé une première unité de production dans l’Est de la France pour pouvoir produire en 2023 plus de 300 kg de H2 par jour ! [13]
3/ L’hydrogène géologique comme future source d’hydrogène ?
L’hydrogène naturel de type moléculaire H2 peut se trouver dans le milieu géologique terrestre. Ainsi à Chimère (Yanartas) en Turquie des gaz s’échappent du sol dont du méthane mêlé à l’hydrogène et brûlent en permanence depuis plus de 2500 ans. Selon les Grecs anciens il s’agirait de l’origine de la flamme olympique ! La formation de l’hydrogène proviendrait d’un dégazage profond provenant du manteau et/ou du cœur de la terre. Un premier puits fonctionne depuis 2012 au Mali et des forages prometteurs (H2 à 98% de pureté !) ont eu lieu notamment en Amérique du Nord en 2019. [14]
L'électrolyse de l'eau
* Le normo-mètre cube (Nm3) est une unité de norme correspondant à une quantité de gaz contenu dans un volume d’un m3 se trouvant dans les conditions normales de pression et de température.
Pour approfondir et illustrer ce sujet :
[1] Le vocabulaire de l’hydrogène de C. Andrieux, L’Actualité chimique n° 466 (octobre 2021) p. 8
[2] Hydrogène, la compétition mondiale a commencé, Numéro spécial commun des revues Challenges et Transitions et Energies d’avril-juin 2021
[3] L’hydrogène vert au secours des renouvelables de J.-C. Bernier, éditorial sur Mediachimie.org (avril 2017)
[4] Qu’est-ce que l’hydrogène vert ? de F. Brénon, Question du mois sur Mediachimie.org (décembre 2019)
[5] Vision de l’hydrogène pour une énergie décarbonée de Xavier Vigor, colloque Chimie et énergies nouvelles (février 2021)
[6] La production d’hydrogène décarbonée et compétitive : un défi technologique à relever de J.-P. Foulon, H. Toulhoat et E. Freund, L’Actualité chimique n° 466 (octobre 2021) p. 11
[7] Site H-Nat 2021
]8] En Vendée, on produit de l’hydrogène vert, « une première mondiale » article de Ouest France (3 septembre 2021)
[9] Filière hydrogène : principaux verrous et intérêt du Power to Gas de J. Deschamps, Techniques de l’Ingénieur (juin 2019)
[10] Les systèmes d’électrolyse de l’eau à membrane échangeuse de protons de S. Germe, F. Fouda-Onana et S. Rosini, L’Actualité chimique n° 466 (octobre 2021) p. 20
[11] Production d’hydrogène par électrolyse de la vapeur d’eau à haute température de J. Mougin, L’Actualité chimique n° 466 (octobre 2021) p. 12
[12] La pyrolyse du méthane : de l’hydrogène « gris » à l’hydrogène « turquoise » de L. Fulcheri, L’Actualité chimique n°466 (octobre 2021) p. 28
[13] Pyrogazéification et thermolyse : vapocraquage de la biomasse de P. Haffner, Colloque Hydrogène décarboné : enjeux et solutions ? Maison de la Chimie (13 juin 2019)
et séminaire Un virage réussi vers la production d’hydrogène Ecole de Paris du management (séance du 27/01/2021)
[14] L’hydrogène naturel, une nouvelle source d’énergie renouvelable de V. Zgonik, L’Actualité chimique n° 466 (octobre 2021) p. 35
Les références [1],[6] [10] [11] [12] [14] sont issues du numéro spécial de l’Actualité Chimique n° 466 (octobre 2021) et téléchargeables, avec l’aimable autorisation de la revue.
Crédits illustration : L’électrolyse de l’eau, Vision de l’hydrogène pour une énergie décarbonée, Xavier Vigor, Colloque Chimie et énergies nouvelles.
La chimie en flux continu consiste à réaliser les synthèses dans des dispositifs traversés par le milieu réactionnel en écoulement dans lesquels on effectue toutes les réactions et les transformations physicochimiques sans isoler les intermédiaires. Elle diffère de la chimie en mode discontinu classique (batch) qui s’effectue dans un réacteur (ballon) suivie des différentes étapes de la synthèse. La chimie en flux continu permet de contrôler précisément les conditions de réaction pour optimiser les rendements et les sélectivités.
La maîtrise de la température réactionnelle qui nécessite d’égaliser les flux de chaleur et les échanges thermiques est très nettement améliorée ici. On peut ainsi calculer qu’un réacteur tubulaire de diamètre de 5 mm montre une excellente aptitude de transfert thermique 100 fois supérieure à celle d’un réacteur tubulaire de 10 cm de diamètre. Des modèles mathématiques montrent que le transfert de matière est un élément important et joue en particulier sur la sélectivité des réactions [1].
La microfluidique s’intéresse aux écoulements dans des canaux de dimension de l’ordre du micron par analogie au monde du vivant. En effet le réseau de la circulation du sang fait intervenir des capillaires sanguins de cette dimension, tout comme dans les plantes le transport de l’eau vers les feuilles s’effectue sous l’action de forces capillaires qui agissent à ces petites échelles [2].
Le développement de la microfluidique a permis de diminuer les quantités des produits à mélanger et rend plus reproductible les conditions expérimentales en contrôlant finement les vitesses des ajouts des réactifs et le temps de séjour dans le microréacteur (donc le temps de réaction) [3].
À ces dimensions les lois de la mécanique des fluides sont celles des écoulements laminaires (fluide dit newtonien) sans aucune turbulence. Il en résulte que la mise en contact de deux liquides se traduit par un mélange uniquement obtenu par un phénomène lent de diffusion. Il est donc nécessaire de concevoir des méthodes de mélange efficace pour créer de véritables « labos sur puce » [4].
Aussi la microfluidique a bénéficié des travaux de G. Whitesides (Université de Harvard) des années 90 sur la lithographie douce qui permet alors de fabriquer des dispositifs microfluidiques en polymère transparent de longueur variant de 10 à 100 µm. Les dispositifs de base sont alors des micro-mélangeurs, micro-générateurs de gradient de concentration, et micro-diffuseurs [2].
À ces dimensions on peut ainsi utiliser des émulsions pour fabriquer une à une des gouttelettes d’un fluide au sein d’un autre fluide non miscible, à des fréquences d’une dizaine de gouttelettes par seconde, créant des trains de gouttes monodispersées et confinées qui circulent à vitesse constante de l’ordre de 1 mmol/s. La goutte devient alors un véritable réacteur chimique ! [5] qui par exemple sous l’effet d’ultrasons éclate et libère le produit formé. Ainsi la combinaison de microgouttes de perfluorocarbone (PFC) avec des ultrasons (US) permet d’abord de déclencher à distance la vaporisation du PFC et ensuite l’ouverture des microgouttes avec libération de leur contenu. Ainsi on peut utiliser des microgouttes pour contrôler à la fois dans l’espace et dans le temps une réaction chimique par exemple la cycloaddition non catalysée entre un azoture et un alcyne conduisant à des médicaments comme la doxorubine libérée au niveau d’une tumeur cancéreuse (leucémie) [6].
La miniaturisation des réacteurs en flux continu rend la fabrication moins onéreuse des produits à forte valeur ajoutée. Ce type de réacteur permet de réaliser des synthèses de chimie fine impossibles dans un réacteur standard. Ainsi l’emploi de « turbo Grignard » (organomagnésien complexé par LiCl) permet dans des conditions de flux continu de réaliser des échanges halogène-métal à des températures nettement plus élevées (allant jusqu’à 95°C) que dans des réacteurs statiques. Des métallations sélectives avec des « superbases » mixtes de lithium et de zinc sur des hétérocycles azotés sont possibles en flux continu avec des rendements dépassant toujours les 90% alors qu’elles ne sont pas possibles dans des réacteurs classiques ou des ballons réactionnels ! [7]
Par ailleurs cela permet d’atteindre des temps de réaction très courts (de l’ordre de la milliseconde), d’où le nom de chimie éclair, et de réaliser des mélanges efficaces pour effectuer des réactions de chimie organique quasi impossibles par la synthèse conventionnelle. En effet il est important de signaler que la sélectivité organique n’est pas liée à la réaction chimique mais plutôt au système : si cela ne change pas les contrôles cinétiques réactionnels, cela influence le cours de deux réactions dans la façon de mettre en contact les réactifs. Mentionnons ainsi que les ortho, méta et para iodophénones d’alkyles dans des conditions de microfluidique sous l’action d’un organolithien donnent une régiosélectivité totale sur le site électrophile du groupement carbonyle ! [8]
Des synthèses de médicaments sont réalisées dans d’excellentes conditions. Ainsi un anticancéreux comme le tamoxifène (cancer du sein) est synthétisé par synthèse organométallique à plus de 220 grammes par jour correspondant à une production de 20 000 doses [9].
En général des réactions de nitration, réduction et de dimérisation sont réalisables industriellement dans des conditions de « flow chemistry » à des températures et des pressions élevées (150°C, 20 bars) avec une accélération d’un facteur 1000 [10].
Il existe des réacteurs photochimiques microfluidiques très performants. Cela permet de réaliser aussi des synthèses de médicaments : l’odanacatib, utilisé pour traiter l’ostéoporose, est ainsi produite avec un rendement de 1g/h au lieu de 1mg/h dans un réacteur classique (batch). Il en est de même pour la camptothécine dans un réacteur à lit plan en flux continu qui est obtenu par ce procédé avec plus 90% de rendement alors qu’en procédé classique (batch), le rendement n’était que de 50% ! [11] La camptothécine est une molécule cytotoxique mais qui intervient dans la synthèse de médicaments anticancéreux.
Des spectres RMN pour analyse en ligne de réaction en flux continu sont réalisés avec des appareils miniaturisés dans des dispositifs portatifs. Il s’agit alors d’appareils à bas champ de 40 à 80 MHz à des prix attractifs de l’ordre de 50.000 à 100.000 euros. La méthode ne nécessite pas de solvants deutérés, mais il faut travailler en solutions concentrées et des recherches pour résoudre les problèmes de sensibilité et de résolution sont requises. Néanmoins un suivi par cette méthode a déjà été développé par exemple pour la neutralisation oxydante des produits toxiques de type « gaz moutarde » [12].
La microfluidique a permis de faire des progrès importants dans le domaine de la formulation. Citons la réalisation des tests immunologiques. Des crèmes à microgouttelettes en suspension peuvent être préservées jusqu’à l’application sur la peau et ont été récemment industrialisées et commercialisées pour des applications en cosmétologie [13].
Des exemples d’industrialisation existent déjà à grande échelle :
- La production de polysulfones en continu avec un dispositif de cisaillement pour diminuer la viscosité du milieu a permis de s’affranchir de l’utilisation de solvants dans un pilote de production de 10 kg/h pour un temps de séjour d’à peine 1 heure ; l’objectif du développement est de passer à une capacité industrielle de 250 tonnes par an ! [14]
- La microfluidique permet aussi de synthétiser des nanomatériaux en contrôlant mieux leur taille, leur forme et leur réactivité. Ainsi la pyrolyse laser permet en flux continu la production de nanoparticules de silicium utilisée dans des batteries [15]. Des nanocristaux de CaCO3, d’une dizaine de nm et d’une aire massique de 50m2/g peuvent être produits à raison de 10 tonnes par an, ceci après un travail de développement industriel de plus de sept années et sont utilisés par exemple dans des administrations de médicaments ! [16]
En conclusion « faire mieux avec moins : la microfluidique ! » [17].

Pour la chimie en flux, nous sommes passés d’un montage dédié (A) à une unité flexible multi-réactionnelle (B) (comparaison 1992-2019). Source : B) www.vapourtec.com in Chimie et nouvelles thérapies (EDP Sciences 2020) p. 235
Pour approfondir et illustrer ce sujet :
[1] Principes théoriques de la chimie en flux de L. Falk et coll., Techniques de l’Ingénieur, fiche J 8025
[2] Microfluidique (PDF) de O. Choffrut, mémoire 2018-2019 ENS
[3] Vidéo en anglais avec un bref résumé et des dispositifs commerciaux de Vapoutec sur le site de la société Vapourtec
[4] La microfluidique : principes physiques et mise en œuvre d’écoulements continus (PDF) 31/03/2016, de O. Français et coll., ENS Paris Saclay
[5] Comment circulent des gouttes dans un laboratoire sur puce ? article de P. Pannizza et coll., Reflets de la Physique n°36 (octobre 2013) pp. 4-9
[6] Réactions chimiques et mélanges locaux induits par ultrasons : vers une chimiothérapie ciblée de M. Bezagu, Thèse Université Pierre et Marie Curie - Paris VI, 2015, NNT : 2015PA066492, tel-01299791
[7] Chimie organométallique en flux continu de P. Knochel et coll., Techniques de l’Ingénieur, fiche J 8030
[8] Chimie éclair et synthèse microfluidique de J. Legros et coll., Techniques de l’Ingénieur, fiche J 8035
[9] Chemistry in a changing world de S. Ley et coll., L’Actualité chimique n° 393-394 (février-mars 2015) pp. 96-101
[10] Chimie fine et pharmacie, de G. Guillamot, conférence vidéo et article du colloque Chimie et Nouvelles thérapies (2019) pp. 227-240 sur le site Mediachimie.org
[11] La photochimie organique et ses applications industrielles de N. Hoffmann, conférence vidéo et article du colloque Chimie et Lumière (2020) pp. 19-35 sur le site Mediachimie.org
[12] Spectre RMN analyse en ligne de réactions en flux continu de P. Giraudeau et coll., Techniques de l’Ingénieur, fiche J 8015
[13] Microfluidique et Formulation de V. Nardello-Rataj et coll., Techniques de l’Ingénieur, fiche : J 8010
[14] Intensification des procédés d’industrialisation de C. Gourdon, Techniques de l’Ingénieur, fiche J 7002
[15] La pyrolyse laser, une méthode industrielle de production de nanoparticules de J.F. Perrin, conférence vidéo et article du colloque Chimie et Nanomatériaux et Nanotechnologies (2019) pages 227-237 sur le site Mediachimie.org
[16] Synthèse de nanomatériaux en dispositifs microfluidiques de M. Penhoat, Techniques de l’Ingénieur, fiche J 8070
[17] Faire mieux avec moins : la microfluidique de S. Descroix et coll., dans le livre « Étonnante Chimie » (CNRS, Editions 2021)
Les références [1], [7], [8], [12], [13], [14] et [16] sont extraites de l’ouvrage collectif coédité par le CNRS et les Techniques de l’Ingénieur (TI) en 2021. Ce fascicule est disponible et pourra être obtenu gracieusement sur demande en signalant l’origine de cette note de ZOOM et en prenant contact avec les adresses suivantes : julien.legros @ univ-rouen.fr ou maud.buisine @ teching.com.
Un pigment est un matériau insoluble dans le milieu dans lequel il est dispersé alors qu’un colorant y est soluble [1] [2].
Les matières colorantes absorbent la lumière dans un domaine de longueur d’onde compris entre 400 et 750 nm. Les origines de la couleur sont liées aux structures chimiques de ces substances [1a]. Pour les composés organiques il s’agit d’une absorption d’un niveau électronique moléculaire à un autre. Pour les composés minéraux ce sont souvent des cations de métaux de transition d’un solide qui sont responsables de l’absorption mais il faut tenir compte de leur environnement anionique (transitions entre les niveaux électroniques des complexes cation/anion ainsi formés). C’est ainsi que l’ion cobalt (II) passe du bleu de cobalt [Co3(PO4)2] au violet clair [Co3(AsO4)2] ; le violet de cobalt est le seul pigment violet de la palette du peintre ! [1a].
Dans les peintures de la grotte de Chauvet découvertes au début des années 2000 et qui datent de 33000 ans environ, s’il est aisé de comprendre que le noir provient du charbon issu de la calcination des os, d’ivoire ou du bois, il n’est pas évident d’expliquer la présence des nuances d’ocre ! Il a été démontré par analyse de diffraction des rayons X au Centre de Recherche et de Restauration des Musées de France (C2RMF) que les pigments ocre sont tous des oxydes de fer : l’hématite (Fe2O3) de couleur rouge et la goethite (FeOOH) de couleur jaune. Dans les deux cas c’est le cation Fe3+ qui se trouve au centre d’un octaèdre dont les six sommets sont respectivement six ions oxyde, et trois ions oxyde et trois ions hydroxyde, les absorptions n’ayant pas lieu aux mêmes longueurs d’onde. La cuisson de la goethite permet sa transformation en hématite et c’est vers 300 - 400°C que l’on obtient les ocres orangés [3] [8].
Le bleu égyptien n’est pas un pigment naturel mais obtenu par chauffage aux environs de 1000°C d’un mélange de calcaire, de silice et de composés cuivreux pour conduire à une masse compacte hétérogène de cuprorivaïte (CaO, CuO, 4 SiO2) et de quartz et tridymite (variétés de silice SiO2) : la nuance de bleu varie avec la température de 900 à 1100 °C et le broyage conduit alors à une couleur bleu clair pour des grains de 20 µm [1].
La couleur bleue (bleu outremer) du lapis-lazuli n’est pas due à l’élément cuivre mais au soufre ! En effet des mesures par RPE (1970) ont mis en évidence l’anion radical trisulfure (S3-), dans une cage d’aluminosilicate type zéolithe, qui absorbe vers 600 nm (dans le domaine du rouge) ce qui explique sa couleur bleue (couleurs complémentaires) [1].
Le bleu de Prusse est un pigment minéral de formule Fe4 [Fe(CN)6, 15 H2O]3 qui cristallise dans le système cubique faces centrées. Depuis la découverte à Berlin par Diesbach en 1706 [5a] il était préparé par distillation du sang en présence de sulfate de fer en milieu alcalin (carbonate de potassium). Actuellement il est préparé à partir de deux solutions aqueuses d’hexacyanoferrate (II) de potassium et de nitrate de fer (III). Il est possible de changer la couleur simplement en modifiant les degrés d’oxydation de l’un des cations. Par exemple sous l’action d’une électrolyse la réduction suivante peut se produire :
K4FeIII [FeII(CN)6]4 + 4 K+ + 4 e- → K8 FeII [FeII(CN)6 ]4
La couleur est variable en fonction du potentiel appliqué à la cathode : -0,2 V (incolore), - 0,6 V (cyan) 1,0 V (vert), 1,5 V (jaune) ! Cela pourrait permettre de créer des vitres pouvant changer de couleur sous l’action d’un courant électrique. Des brevets ont été déposés mais sans développement à ce jour [5b].
Le bleu de Prusse intervient dans la composition de cathodes en particulier sous la forme NaxMaNbFe(CN)6 des batteries sodium–ion (Na–ion), où M et N sont des éléments de transition avec x voisin de 1,9 et a et b ≤ 1. La batterie au sodium est moins onéreuse que celle au lithium et offre une solution durable au stockage de l’énergie avec des dizaines de milliers de cycles de décharge/charge, chaque cycle durant quelques minutes ; elle est développée actuellement par la Société Natron Energy en Californie [6].
La mauvéine est un pigment découvert par hasard par Perkin en 1856 à Londres, alors qu’il cherchait une synthèse de la quinine… qui permettait de traiter la malaria ! L’analyse en 2007, a montré qu’il s’agissait ici d’un mélange de quatre molécules organiques de couleur mauve appelées mauvéines A, B1, B2 et C. Ainsi la Reine Victoria en Angleterre et l’Impératrice Eugénie ont porté de somptueuses robes de soie colorées avec de la mauvéine ! [7] [8]
La poudre de pigment n’est pas applicable directement sur un support : pour assurer l’adhésion, les particules doivent être dispersées dans une substance appelée liant.
Dans la peinture à l’eau le liant a été d’abord de l’eau à laquelle on ajoutait de la gomme arabique (molécules de sucres associées solubles dans l’eau) pour obtenir des aquarelles ou des gouaches selon la quantité de gomme ajoutée. Puis, à partir du XVe siècle, on a ajouté à l’eau du jaune d’œuf. Ce dernier renferme 30% de lécithine qui est un phospholipide, molécule contenant des chaînes hydrocarbonées apolaires lipophiles avec des extrémités chargées hydrophiles ; on obtient une émulsion dans laquelle les particules de pigments (composé ioniques) sont alors dispersées sans pouvoir s’associer en agglomérats qui seraient inutilisables pour la peinture. On peut remplacer le jaune d’œuf par de la glycérine [1a].
Dans la peinture à l’huile, le liant est surtout l’huile de lin. Son usage a été introduit par les frères Van Eyck au XVe siècle. L’huile de lin est un mélange de triglycérides, triesters du glycérol et de trois acides gras insaturés (dans ce cas les acides linolénique, linoléique et oléique). La pâte contenant les pigments dispersés dans l’huile est conservée dans des tubes. Étalée sur la toile, la peinture « sèche » : en fait elle donne une réaction de polymérisation en présence de l’oxygène de l’air grâce aux doubles liaisons C=C insaturés pour donner un réseau 3D par réticulation et donc un film résistant et souple [1a].
Mais un grand changement s’est opéré avec les peintures acryliques dans les années 1950. Cette découverte est due à des chimistes de Mexico : le liant est une émulsion d’eau et de résines acryliques (solubles en milieu aqueux en raison des parties protiques ou polaires) issues de la polymérisation de dérivés acryliques monomères de type CH2=CH-CO2H ou CH2=CH-CO2R qui conduisent à des films de très grande élasticité avec un temps de séchage bien plus court. Elles sont moins sensibles au vieillissement [1a].
Le vieillissement de la peinture des tableaux peut correspondre à des phénomènes d’oxydation. Par exemple la couleur jaune utilisée par Van Gogh était du sulfure de cadmium qui s’oxyde à l’air pour donner des taches blanchâtres de sulfate de cadmium selon l’équation : Cd S (jaune) + O2 → Cd SO4 (blanc) [1b].
Ce pigment toxique (car il contient du cadmium) n’est plus autorisé depuis les directives européennes de 1996 ; cela explique l’apparition récente de pigments à base de sulfure de cérium et de de sodium [8].
Mais le vieillissement peut aussi provenir des réactions d’oxydation photochimique : ainsi la laque géranium (par analogie avec la couleur de la fleur !) utilisée par Van Gogh « passe avec la lumière » et se décolore progressivement. Une analyse par microscopie électronique à balayage a montré la présence d’atomes de brome caractéristiques de la molécule d’éosine [9]. L’éosine absorbe dans le vert à 529 nm. On montre de plus par voltamétrie cyclique que le potentiel redox de l’éosine à l’état fondamental est de 0,78 V mais qu’il s’abaisse à – 1,11 V lorsque l’éosine est à l’état excité, ce qui rend donc l’éosine plus sensible à l’oxydation par l’oxygène [10].
La connaissance des pigments utilisés par un peintre à une certaine période de sa vie permet de dater et donc d’authentifier un tableau. Le développement de l’instrumentation - du pinascope (premier petit microscope utilisé pour l’examen scientifique des peintures) du Dr Pérez des années 30 aux méthodes actuelles de microscopie électronique à balayage couplées avec la diffraction et la fluorescence X - a révélé des fraudes et des scandales retentissants [9].
Ainsi Van Meegeren un peintre restaurateur hollandais avait vendu à Hermann Goering un tableau de Vermeer (peintre hollandais du XVIIe siècle) représentant Marie-Madeleine lavant les pieds du Christ et authentifié par des experts de l’époque… Il fut arrêté à la fin de la guerre et pour « se disculper », il a avoué la falsification en repeignant le tableau devant les enquêteurs. Pour améliorer sa technique (pour rendre ses faux encore plus vrais !) il remplaçait l’huile par des résines acryliques… mais s’il veillait à n’acheter que des pigments purs, un marchand de couleurs avait ajouté, en oubliant de le lui signaler, quelques pigments supplémentaires et en particulier du bleu de cobalt synthétisé par Thénard bien après la mort de Vermeer… en 1799 ! [11]

Image d'illustration
Pour approfondir et illustrer ce sujet :
[1a] La chimie crée sa couleur… sur la palette du peintre de B. Valeur, article et conférence-vidéo du colloque La Chimie et l’Art (2009) sur Mediachimie.org
[1b] Matériaux du patrimoine et altération. Analyses par rayonnement synchrotron de K. Janssens, article et conférence-vidéo du colloque La Chimie et l’Art (2009) sur Mediachimie.org
[2] Les pigments et les colorants : on en parle ? de M. Jaber et Ph. Walter, L’Actualité Chimique n°444-445 (octobre-novembre 2019) p. 13
[3] Identifier les pigments et comprendre leurs propriétés à partir de la diffraction des rayons X de Ph. Walter et coll., L’Actualité Chimique n°387-388-389 (juillet-août-septembre 2014) p. 170
[4] Les couleurs à l’époque de Toutânkhamon de B. Valeur, L’Actualité Chimique n°444-445 (octobre-novembre 2019) p. 10
[5a] La première couleur artificielle : le bleu de Prusse de Catherine Marchal anecdocte et vidéo sur Mediachimie.org
[5b] Toutes les couleurs du bleu de Prusse de G. Fornaseri et coll., L’Actualité Chimique n°444-445 (octobre-novembre 2019) p. 21
[6] L’actualité du solaire juillet 2020
[7] Des matériaux, patrimoines de l’humanité ? Préserver et transmettre une part de l’histoire de la chimie de Ph. Walter, article et conférence du colloque Chimie et Alexandrie (2019) sur site mediachimie.org
[8] Comment la synthèse ratée d’un médicament conduit à un colorant industriel : la mauvéine de B. Bodo et G. Emptoz, anecdote et vidéo sur Mediachimie.org
[9] Histoire secrète des chefs d’œuvre (C2RMF) de D. Dubrana, Editions SPE BARTHELEMY (2001), un beau livre !
[10] Les colorants et la lumière pour transformer la matière N. Hoffmann et coll., L’Actualité Chimique n°444-445 (octobre-novembre 2019) p.38-43
[11] L’Art-Chimie de Ph. Walter et F. Cardinali, Éditions Michel de Maule / Fondation de la Maison de la Chimie (2013), un autre beau livre !
Comment améliorer le rendement d’une réaction de la chimie organique renversable et s’accompagnant de formation d’eau comme produit secondaire ? En utilisant un tube décanteur de Dean Stark que l’on intègre au montage à reflux.
Sur l’exemple d’une estérification, cette vidéo présente le matériel, le montage à réaliser au laboratoire, le choix du solvant et comment mener à bien l’expérience. Dans une 2e partie, le principe théorique faisant appel au diagramme liquide vapeur d’un mélange binaire de deux constituants non miscibles à l’état liquide est développé. Cette vidéo sera utile aux élèves des classes scientifiques de l’enseignement supérieur.
 |
Le génie des procédés
|
Le génie des procédés
Rubrique(s) : Zoom sur...
Les industries de transformation de la matière telles que la chimie, la pharmacie, la métallurgie, les IAA (Industries Agro-Alimentaires)… et les industries de l’énergie mettent sur le marché des produits dont la fabrication nécessite un procédé, d’où leur nom générique d’industries de procédés (Process Industries). […]
Les industries de transformation de la matière telles que la chimie, la pharmacie, la métallurgie, les IAA (Industries Agro-Alimentaires)… et les industries de l’énergie mettent sur le marché des produits dont la fabrication nécessite un procédé, d’où leur nom générique d’industries de procédés (Process Industries).
1. Un exemple
Le cas de l’aspirine (acide acétylsalicylique), produit plus que centenaire, est intéressant. C’est en octobre 1897 que Félix Hoffmann fait la synthèse d’un produit pur et stable dont la société Bayer en 1899 prend le brevet et dépose la marque sous la dénomination d'Aspirin [1].
La dernière étape de la synthèse consiste en la réaction de l’anhydride acétique sur l’acide salicylique (figure 1).

Figure 1 : Synthèse de l’aspirine
La figure 2 schématise à titre purement indicatif le procédé industriel qui comprend les étapes suivantes : réaction, filtration, cristallisation, séparation des cristaux, séchage, suivies de la formulation pour la fabrication des tablettes par compression de l’acide acétylsalicylique avec des adjuvants (excipients).

Figure 2 : Schéma simplifié de la synthèse de l’aspirine (DR : L. Amann)
Un procédé est ainsi une succession d‘opérations physico-chimiques que des professeurs du MIT, au début du XXe siècle, ont dénommé Opérations Unitaires [2] (Unit Operations) et qui sont autant de briques technologiques. Les Opérations Unitaires mettent en œuvre du matériel et des équipements qui, tout en assurant la même fonction, peuvent être de nature différente. Par exemple, un filtre peut être rotatif sous vide, à bande, à plateaux, à manches…
2. La France et le Génie des Procédés (GP)
Le Génie Chimique, GC, ou Chemical Engineering, est né au MIT à la fin du XIXe siècle et a contribué à l’extraordinaire développement de l’industrie chimique et pétrolière. Les professeurs Joseph Cathala et Maurice Letort après des séjours aux États-Unis introduisent cette science en France à Toulouse (IGC devenue ENSIACET) et à Nancy (ENSIC) après la Deuxième Guerre mondiale. Le Professeur Jacques Villermaux de Nancy, un visionnaire, partant du constat que les Techniques du GC s’appliquent à toutes les industries de procédés proposera le terme « Génie des procédés (GP) » en vigueur en France à ce jour. Il est un des fondateurs en 1987 de La SFGP (Société Française du Génie des Procédés) qui en donne la définition suivante :
Le GP est une science d’intégration, une science à part entière qui regroupe les Sciences de l’Ingénieur, les pratiques et méthodes relatives à l’étude, la conception, l’optimisation et la mise en œuvre des procédés de transformation de la matière et de l’énergie par voie chimique, physique ou biologique.
3. LE GP et le processus d’industrialisation
L’Ingénieur de procédés est le chef d’orchestre du processus d’industrialisation qui consiste à définir, construire, démarrer et faire fonctionner l’outil industriel.

Figure 3 : Représentation du processus d’industrialisation. Source : « Chimie pour un développement durable » [3]
La figure 3 schématise le processus d’industrialisation : une suite de processus qui part des études en laboratoire pour aboutir à un atelier qui délivre un produit commercialisable.
Ce processus comprend deux phases distinctes : une phase d’étude et de développement qui, si les crédits d’investissement sont accordés, est suivie d’une phase d’ingénierie de réalisation qui voit la construction de l’atelier, son démarrage et la mise en production.
L’Ingénieur de Procédé est au cœur de ce processus. Il commence par dialoguer avec les chercheurs pour définir ce que l'on appelle les bases de l’industrialisation : choix des conditions de réaction (catalyseur, température, pression, sélection des matières premières et des solvants). Suit alors la sélection du schéma de procédé avec ses opérations unitaires tenant compte des données cinétiques et thermodynamiques. Il décide s’il faut passer par une phase de pilotage avant de passer à la phase Ingénierie de réalisation qui est une phase lourde. De tout ce travail de recherche et d’études en amont découlera la réalisation industrielle.
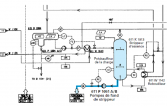
Son travail consiste alors à l’établissement des Schémas de procédés, PFD (Process Flow Diagram), des bilans matières et de chaleur (bilan enthalpique), à définir la nature des matériaux à mettre en œuvre, à identifier l’équipement principal (réacteur, colonnes à distiller, échangeurs de chaleur…) et à définir l’instrumentation (voir figure 4). Suivent les Schémas TI (Tuyauteries et Instruments), P&ID (Piping and Instrumentation Diagram) ainsi que la définition du matériel (Feuilles de spécifications) (*), et de tout ce qui sera nécessaire à l’INGÉNIERIE pour construire l’outil de production répondant à des critères de fiabilité, d’économie, de sécurité et d’environnement. Il contribue au calcul du prix de revient du produit fabriqué élément essentiel de détermination de la rentabilité d’un projet à partir du volume et du montant des ventes [4].
 |  |
| Figure 4 : Exemple de procédé d’un strippeur d’essence (schéma partiel). Source : Techniques de l’Ingénieur AG 3300 MC CHARRIER | Figure 5 : Vue en élévation 3D de l’installation dont la fig. 4 représente le procédé TI AG 3300 MC CHARRIER |
L’ensemble du processus de l’ingénierie de réalisation fait appel à une vingtaine de métiers (femmes et hommes) : techniciens et ingénieurs de procédés, de projet, planificateurs, estimateurs, acheteurs, chef de chantier, instrumentistes, automaticiens et à de nombreux corps de métiers (génie civil, chaudronnerie, tuyauteries, machine tournantes, électricité…).
Les industries de procédés mettent en jeu un grand nombre de procédés différents caractéristiques de chaque filière (chimie, pharmacie, agroalimentaire…). La voie d’accès, les volumes, ainsi que températures et pressions mises en jeu donnent à l’atelier sa caractéristique. Certains procédés chimiques sont remplacés par des procédés par voie biotechnologique tout particulièrement en pharmacie [3]. Donc autant de compétences de cœur (Core competencies) différentes.
4. Le GP à l’heure de la révolution numérique
Le GP, dès les années 60, a bénéficié de l’informatique industrielle. L’encre de Chine et les tables à dessin vont laisser la place aux ordinateurs ; fini les calculs fastidieux ! Une multitude de logiciels sont utilisés pour définir les nappes de tuyauteries, l’implantation du matériel, construire des maquettes virtuelles (jumeau numérique) qui serviront à vérifier l’ergonomie des postes de travail et les conditions de maintenance.
La puissance sans cesse accrue des ordinateurs permet de modéliser, simuler et optimiser les procédés ; c’est le domaine de la MSO (Modélisation, Simulation, Optimisation) [5] [6].
La révolution numérique amène des changements profonds dans la conception des usines et leurs opérations ; jumeau numérique, robotique, cobotique (robot soulageant le travail humain) et exosquelettes modifient le travail des opérateurs qui peuvent bénéficier de la réalité augmentée, de la réalité virtuelle via tablette ou smartphone. Tout peut être connecté à tout par l’Internet des Objets (IOT) qui génèrent des données (Big Data) que les ordinateurs peuvent traiter en temps réel. Toutes ces avancées numériques et ces outils font dorénavant partie de la Boite à outils (ToolBox) de l’ingénieur moderne ; ils sont en progrès constants.
5. Les nouvelles exigences de la société et des consommateurs
La société veut aujourd’hui des usines avec une « empreinte carbone » minimale respectueuse de l’environnement, apportant de la valeur ajoutée à la société aussi bien qu’aux clients. Le consommateur veut des produits éco-conçus, durables avec une analyse du cycle de vie (ACV) transparente [7], [3].

Figure 6 : Le cycle du produit
L’entreprise est née de la révolution industrielle ; elle risque ses capitaux pour faire du profit. Depuis des années elle doit tenir compte de la notion de RSE (Responsabilité Sociétale de l’Entreprise). La RSE c’est l’application du concept de développement durable au fonctionnement de l’entreprise (voir figure 6).
Depuis quelques années s’impose la notion d’entreprise à mission ; notion légale par laquelle l’entreprise affiche son engagement social pour un « Bien commun », notion définie par Jean Tirole, prix Nobel d’Économie.
6. L’usine du futur à l’ère des évolutions écologique, énergétique et numérique
Depuis quelques années est apparue la notion d’usine du futur ou usine 4.0 suivant les pays ; une usine qui, à l’instar de l’éthique de l’entreprise qui la possède, répond au concept du développement durable que la figure 7 schématise.
L’impact de l’usine sur son environnement et en premier lieu sur ses opérateurs et les riverains va dépendre du procédé mis en œuvre et de sa gestion ; accidents, épanchements sont à éviter.
Cependant toute activité humaine a un impact sur l’environnement au sens le plus large ; l’impact Zéro comme le risque zéro n’existe pas. Le point de fonctionnement du triangle de la figure 7 représente le meilleur compromis entre les 3 P : People, Profit, Planet.

Figure 7 : le développement durable représenté par les « 3P »
Ce point de fonctionnement est défini à partir de métriques (Metrics) qui accordent des poids différents à l’énergie, à la main d’œuvre et aux rejets suivant les situations. Par exemple au Sahel la contrainte sur l’eau étant majeure, on privilégiera surtout un procédé à faible consommation d’eau, l’énergie pouvant d’être d’origine solaire.
7. Les procédés chimiques s’améliorent ou se transforment pour répondre aux principes de la « chimie verte » [3]
Les produits, « raison d’être » du système productif, doivent être éco-conçus en utilisant dans la mesure du possible des matières premières (MP) biosourcées [7] si l’économie le permet et favoriser une économie circulaire au lieu d’une économie linéaire (on produit, on utilise, on jette). L’économie circulaire [8] favorise la « frugalité en MP, la réutilisation des produits autant que de possible et l’utilisation de leurs composants en fin de vie. C’est la règle des 3R : Réduire, Réutiliser et Recycler.
8. Entreprise, outil industriel et produit forment un tout
À l’heure où notre société doit faire face à des défis vitaux, stress hydrique, urbanisation, migrations, changement climatique, l’Ingénieur de procédé contribue aux choix technologiques. Son rôle sociétal s’affirme de plus en plus. Il le fait dans un monde de compétition effrénée où la technologie est devenue une arme économique et où les demandes sociétales médiatisées se vivent dans l’immédiat.
Il ne faut pas perdre de vue qu’il est indispensable de tenir compte de l’ensemble des conditions économiques et techniques associées à une demande de produit. Par exemple l’utilisation de l’hydrogène n’apporte de réduction de CO2 que s’il est fabriqué par hydrolyse de l’eau avec une électricité elle-même décarbonée. En effet l’hydrogène obtenu par vaporéformage (action de la vapeur d’eau sur des hydrocarbures fossiles) produit du CO2.
L’ingénieur de procédés doit tenir compte de ces changements et des contraintes afférentes qui sont aussi des opportunités. Le génie des procédés a considérablement évolué au cours de la dernière décennie ; nul ne doute qu’il évoluera encore à l’instar de la révolution numérique dont on ne voit pas ni la fin ni les conséquences.
(*) Par exemple dans le cas d’une distillation il est nécessaire de déterminer les caractéristiques de la colonne qui sera la mieux adaptée (diamètre, nombre et type de plateaux ou hauteur de garnissage, vrac ou rangé) ou encore le choix de l’agitateur sera fondamental [2] pour répondre à la fois au mélange efficace des réactifs, au transfert de chaleur tout en respectant la morphologie des cristaux en cristallisation ou en minimisant le stress des bactéries en fermentation.
[1] Du saule à l’aspirine de Olivier Lafont, Revue d'histoire de la pharmacie, 94e année, n° 354 (2007) pp. 209-216
[2] Quelques vidéos illustrant les opérations unitaires : Fluidisation gaz-solide et Agitation
[3] Chimie pour un développement durable (SECF)
[4] Pour découvrir les métiers liés au génie chimique et au génie des procédés consulter sur Mediachimie dans l’espace Métiers le domaine d’activité Procédés
[5] La modélisation numérique et l’ingénierie de l’environnement, L'Actualité Chimique n° 450 (avril 2020) p. 19
[6] La modélisation moléculaire s’invite dans l’industrie, de Frédéric Biscay et al., L'Actualité Chimique n° 353-354 (juin-juillet-août 2012) p. 66-73
[7] Valorisation biologique des agro-ressources de Pierre Monsan, in La chimie et la Nature (EDP Sciences, 2012) p. 253
[8] Les chimistes dans : l'économie circulaire (Mediachimie)
Pour en savoir plus
1) Perry : Manuel des ingénieurs-chimistes (McGraw-Hill, 9e éd., 2018). La « Bible de l’Ingénieur de procédés ».
2) J.-P. Dal Pont et M. Debacq : Les Industries de procédés, Vol. 1, Vol. 2 (Éd. ISTE 2020)
3) C. Cogné, M. Debacq, H. Desmorieux, N. Fatah, N. Regnier, É. Schaer et M. Tourbin. SFGP : Ressources pédagogiques en ligne sur le portail du génie des procédés.
4) Techniques de L’Ingénieur. Procédés Chimie - Bio – Agro : description de toutes les Opérations Unitaires (970 articles).
Les méthodes de dosages par titrage sont de plus en plus remplacées par des méthodes de dosage dites par étalonnage.
Le microcontrôleur « Arduino » est relié à des diodes électroluminescentes (LED). Des kits commerciaux proposent souvent 4 LED de couleurs différentes (bleu, vert, jaune et rouge). Une simple intercalation d’un récipient contenant une solution colorée permet l’extinction de diodes à mettre en relation avec l’observation de la couleur fournie par l’œil de l’observateur (couleur complémentaire). Comme ce microcontrôleur permet de mesurer une tension entre 0 et 5 V en un point d’un circuit électrique avec un convertisseur alors il peut détecter un signal lumineux arrivant sur un capteur tel qu’une photodiode. L’auteur aborde de manière très claire la discussion des mesures de l’absorbance Io traditionnellement appelée « mesure du zéro » qui dépend de la géométrie de la cuve, de son épaisseur et de la solution qui doit « tout contenir sauf le colorant » ! Plusieurs solutions d’étalonnage sont préparées et une relation affine modélise l’absorbance en fonction de la concentration la solution, mais là aussi une discussion très intéressante a lieu sur la détermination de l’incertitude sur la concentration retrouvée par la méthode d’étalonnage : un guide EURACHEM indiqué dans la bibliographie en version traduite en français en 2016 pourra être consulté avec profit.
Source : L’Actualité chimique n° 452 (juib 2020) pp. 29-34
 |
Les vaccins
|
Les vaccins
Rubrique(s) : Zoom sur...
Les vaccins soulèvent des questions auxquelles ce zoom essaie d’apporter des éclaircissements.
- Quelle est la différence entre un agent pharmacologique à visée thérapeutique (médicament) et un vaccin ?
- Quels sont les concepts d’élaborations des vaccins existants ayant fait leur preuve ?
- Sur quelles bases scientifiques les nouveaux vaccins à ARN messager proposés sont-ils conçus ?
- Quelles sont les attentes en termes d’activité, durée d’activité versus toxicité en moyen long terme ?
- Le cas des vaccins à ARN modifié ou à ADN ; les questions qui se posent
- Propositions […]

